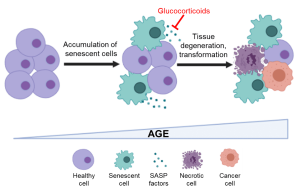
Auswirkungen von Glucocorticoiden auf das Seneszenz-bedingte Inflammaging. Erstellt mit BioRender
Grafik: Aishwarya Iyer-BierhoffProjektleiter: Thorsten Heinzel
Stress führt zu dauerhaften, funktionellen epigenetischen Veränderungen, die sich auf die Gesundheit und Lebensspanne auswirken. Die Hypothalamus-Hypophysen-Nebennieren-Achse (HPA-Achse) ist der wichtigste neuroendokrine Regelkreis, der die Anpassung an Stress initiiert und reguliert und so das Überleben fördert. Beim Auftreten von Stressoren, wie z. B. einem Immunstimulus, löst die HPA-Achse die Freisetzung von Glucocorticoiden (GCs) wie Cortisol aus. Cortisol bindet an den Glucocorticoidrezeptor (GR) in den Zielzellen und löst eine entzündungshemmende transkriptionelle Antwort aus, um die Homöostase wiederherzustellen. Daher stärken geringe Mengen akuten Stresses die Resilienz. Während des Alterns häufen sich seneszente Zellen, die einen pro-inflammatorischen sekretorischen Phänotyp (SASP) aufweisen und einen chronischen, systemischen Entzündungszustand fördern, der als Inflammaging bezeichnet wird. Dieser Zustand beschleunigt altersbedingte Komorbiditäten wie Gebrechlichkeit, neurodegenerative und kardiovaskuläre Erkrankungen.
Wie sich die altersbedingte Deregulierung der HPA-Achse und die GC-GR-Signaltransduktion auf das Inflammaging auswirken, ist noch unklar. Darüber hinaus moduliert GR die Chromatinlandschaft in der Nähe der DNA-Methylierungsstellen und stellt damit eine Verbindung zwischen Stressreaktion und epigenetischem Alter her. In dieser Studie werden wir die Beziehung zwischen epigenetischem Alter, Cortisol- und pro-inflammatorischen Zytokinspiegeln und der GR-Expression in alternden menschlichen Kohorten untersuchen. Anhand von Zellkulturen und Tiermodellen sollen die molekularen Mechanismen erforscht werden, die der GR-vermittelten epigenetischen Regulierung von Seneszenz und Inflammaging zugrunde liegen. Darüber hinaus werden wir untersuchen, ob entzündungshemmende Maßnahmen mit synthetischen Glucocorticoiden als Senomodulatoren eingesetzt werden können, um den SASP zu unterdrücken und die Lebenserwartung in Modellorganismen zu verbessern.
Mehr InformationenExterner Link
Doktorandin: Sandra Weber
Postdocs: Maren Godmann, Aishwarya Iyer-Bierhoff